Immune Deficiency Mouse Models Strains
免疫缺陷小鼠是指一种或多种免疫系统组成成分缺陷的小鼠。随着基因编辑技术的不断发展,越来越多的免疫缺陷小鼠品系被研发出来,在免疫学,传染病学,肿瘤学,干细胞生物学等研究领域中发挥着越来越重要的作用。本期小编将对免疫缺陷小鼠的前世今生进行全面盘点。
免疫缺陷小鼠发展历史
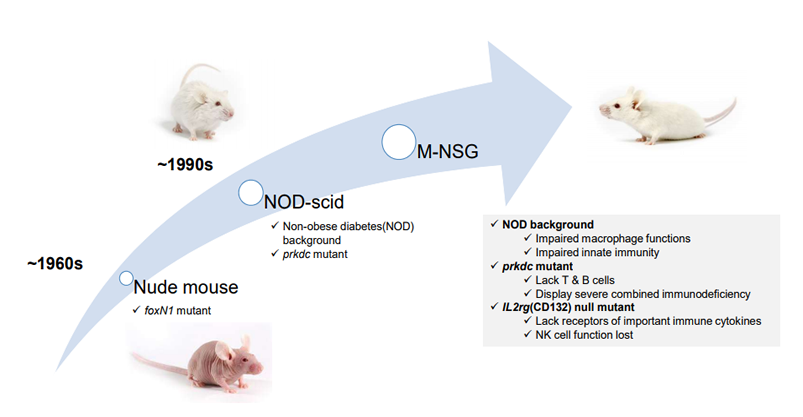
自上世纪60年代,裸鼠作为第一类免疫缺陷品系出现,后面又经历了90年代免疫缺陷程度更高的NOD/SCID小鼠被开发出来,直到21世纪初,科学家们在NOD/SCID小鼠品系引入IL-2Rγ的突变,进而产生了目前来讲免疫缺陷程度最高的NSG小鼠或NOG小鼠(Fig1)。在这个漫长的历程中,也产生了很多衍生品系,有不少直到今天也在广泛使用,下面小编将逐一介绍。
1、Nude小鼠(裸鼠)
1962年,第一个免疫功能障碍的小鼠在英国的Ruchill医院被发现。它们由于浑身不长毛,所以被叫做裸鼠(Nude)。裸鼠的Foxn1基因缺陷,缺乏功能性胸腺和T淋巴细胞,导致它们的适应性免疫应答(包括T细胞介导的免疫应答和辅助T细胞介导的抗体形成)是有缺陷的。这使得它们通常不排斥同种或异种移植物,因此裸鼠开始被用作人肿瘤异种移植物的受体。不过,裸鼠仍具有B细胞和NK细胞(NK细胞比野生型小鼠更活跃),完整的先天免疫一定程度上限制了人类癌症移植的选择。此外,裸鼠随着年龄的增长会出现T细胞的渗漏。
2、SCID小鼠
严重联合免疫缺陷小鼠 Severe Combined Immunodeficient Mice
1983年,Bosma(美国Fox Chase癌症研究所)在CB17近交系小鼠中发现位于16号染色体上的Prkdc基因存在隐性突变,并首次描述了缺乏功能性T和B淋巴细胞的严重联合免疫缺陷(SCID)小鼠。SCID小鼠外观与普遍小鼠无差异,体重发育正常,但是胸腺和外周淋巴组织严重萎缩。SCID小鼠Prkdc的缺失导致可变(V)、多样性(D)、连接(J)区段无法正常重组。 SCID小鼠最初用作人造血干细胞(HSCs)和外周血单核细胞(PBMC)移植的受体。与裸鼠相比,SCID小鼠的人类肿瘤植入效率更高。不过,人血细胞和肿瘤细胞的移植效率并没有预期的那么高。这是因为SCID小鼠残存有NK细胞、补体及髓系细胞的正常免疫,阻止了人类细胞的归巢和维持。SCID小鼠自发性T细胞淋巴瘤(主要在胸腺)的发病率在15℅左右。
3、RAG-/-小鼠(重组激活基因缺失小鼠)
1992年,缺失重组激活基因(Rag-/-)的免疫缺陷小鼠模型问世。重组激活基因包括Rag1和Rag2两种基因,都是TCR和免疫球蛋白 V(D)J重组所必需的,任一基因的缺失都会导致T细胞和B细胞的缺乏。Rag1-/-和Rag2-/-小鼠的特征基本相似。与SCID小鼠相比,Rag2基因缺失能更早且更完全地阻断T和B细胞分化。不过,Rag-/-小鼠保留了较高水平的NK细胞,在一定程度上也限制了人HSC细胞的移植。(品系详情页)
4、NOD-SCID小鼠
非肥胖型糖尿病/重症联合免疫缺陷小鼠 nonobese diabetic severe combined immunodeficiency
1980年, Makino(日本Shionogi公司)发现非肥胖糖尿病(NOD)小鼠患有由T淋巴细胞浸润和胰岛β细胞破坏引起的糖尿病,同时还伴有多种免疫异常,包括补体缺失和NK、巨噬细胞和树突状细胞功能受损等。
1995年,Shultz通过杂交NOD和SCID小鼠建立了NOD-SCID小鼠。 NOD-SCID小鼠不会发生糖尿病,缺乏T细胞和B细胞,同时具备固有免疫缺陷,因此成为人类造血干细胞和人类实体瘤移植的更好的受体。此外,Shultz等研究发现,SCID小鼠免疫渗漏高达90%,而NOD-scid小鼠则低于10%。NOD-scid小鼠一度成为造血细胞研究中应用最广、最为重要的移植模型。
5、IL2rg-/-小鼠
干扰白细胞介素2 (interleukin2, IL-2)受体gamma链 (IL-2Rγc) 是形成高亲和力受体的重要组成部分,能编码重要的信号通路组成因子(如细胞因子IL-2、IL-4、IL-7、IL-9、IL-15和IL-21),这对于淋巴细胞和NK细胞的发育至关重要。1995年,通过靶向敲除IL-2Rγc基因,获得了IL2rg-/-小鼠。它们的T细胞和B细胞发育和功能严重受损,且NK细胞发育被完全阻断。IL2rg-/-小鼠的产生使更多淋巴细胞缺陷小鼠模型成为可能,可以大大降低人体细胞和组织的排斥率。
IL-2Rγ与Jak3激酶相互作用进行信号转导,因此,Jak3缺失的Jak3-/-小鼠与IL2rg-/-小鼠类似,也缺乏NK细胞且T、B淋巴细胞减少。
6、NSG/NRG/BRG小鼠
2002至2005年,多个实验室分别繁育出了多种带有IL2rg-/-的免疫缺陷小鼠,其中应用最为广泛的几个下小鼠品系为:NOG/NSG小鼠(NOD-SCID IL2rg-/-)、NRG小鼠(NOD-Rag1-/- IL2rg-/-)、BRG小鼠(BALB/cA-Rag2-/- IL2rg-/-)。
正如我们之前提到的,IL-2Rγ缺陷使小鼠接受人HSC和外周血的移植效率远远高于之前的免疫缺陷小鼠。NOG和NSG小鼠是由日本(2002年)和美国(2005年)的实验室分别获得的,都是通过NOD-scid小鼠与IL2rg-/-小鼠交配繁育产生,表现为T、B细胞和NK细胞功能性缺失,是目前人源化组织最理想的受体小鼠。NOG与NSG小鼠的区别在于,NOG小鼠缺失IL-2Rγ胞内结构域,而NSG小鼠则完全缺失IL-2Rγ。
由于种种原因,NSG小鼠目前在国内并无途径进行购买,为解决客户对该类品系的需求,南模生物自主研发了M-NSG小鼠,该品系是在NOD-SCID小鼠基础上敲除Il2rg基因,与NSG或NOG小鼠一样,缺乏成熟的T、B细胞和NK细胞,是目前免疫缺陷程度最高的小鼠之一。(品系详情页)
NRG小鼠与NSG小鼠非常类似,是由Rag1基因缺失代替scid突变,可以克服scid突变引起的一些不足,如:对辐照敏感。BRG小鼠是在BALB/c背景的小鼠中引入Rag1-/-或Rag2-/-突变以及IL-2Rγ缺失,表现为T、B细胞缺失和NK细胞无活性。NRG小鼠的人HSC细胞植入率比BRG高,主要的原因是NOD背景小鼠的SIRPα带有突变,可以结合人源CD47,抑制巨噬细胞对人源细胞的吞噬作用。
7、B-NDG 小鼠
B-NDG小鼠是百奥赛图自主研发的重度免疫缺陷小鼠。其在NOD-scid小鼠背景上又敲除了IL2rg基因,小鼠表现为缺乏成熟的T、B、NK细胞,是目前国际公认的免疫缺陷程度高、适合人源细胞或组织移植的工具小鼠,已被广泛应用于人体免疫系统重建。
虽然利用NOD-scid-IL2rg null这类小鼠尽管进行人免疫重建已经比较成功,且此类模型也被广泛的用于人免疫系统的研究,但是这类小鼠造血细胞的维持、分化功能以及免疫细胞的发育是受限的。为了解决这一问题,百奥赛图在B-NDG小鼠的基础上,又开发了一系列衍生产品,为人类肿瘤临床治疗研究提供了重要的工具和保障。
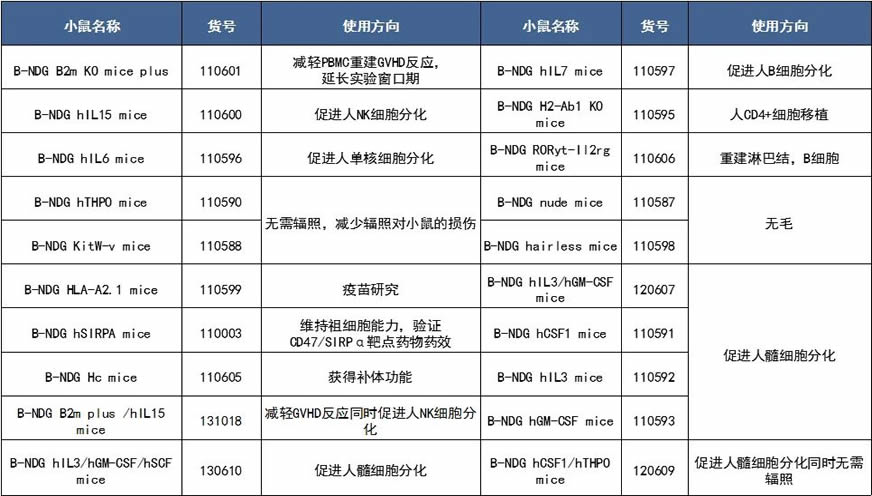
家族族谱:百奥赛图在 B-NDG 基础上进行持续的研发,开发出一系列免疫缺陷小鼠,如减轻 GvHD 的B-NDG B2M KO Plus,支持 NK 细胞发育的 B-NDG hIL15,不依赖辐照的 B-NDG hTHPO 等一系列 B-NDG 二代产品鼠,以满足不同的肿瘤免疫治疗策略中的临床前动物模型需求。
B-NDG鼠应用举例:
对B-NDG、NOD-scid、BALB/c Nude小鼠通过尾静脉注射相同数量(5 × 105)的Raji细胞,后在不同的时间点记录并分析小鼠的如下各种指标。
A.细胞接种后记录小鼠生存情况,绘制Kaplan-Merier生存曲线。
B.细胞接种后每周小鼠体重变化(g),并计算出相对于接种当天的相对体重。
C.小鼠外周血中人源细胞百分率变化。接种Raji细胞后,每周通过眼眶静脉丛采取100 μl全血,提取DNA,通过q-PCR技术检测小鼠外周血中人源细胞比率。
D.接种Raji细胞后小鼠肝脏对比。接种后待小鼠体重下降超过30%后执行安乐死并解剖脏器,进行拍照。
E.接种Raji细胞后小鼠脏器免疫组化染色。一抗为鼠抗人线粒体膜蛋白抗体。
- 利用B-NDG小鼠进行抗人CD47抗体药效验证实验:
将人淋巴B-luciferase-GFP Raji细胞尾静脉注射B-NDG体内,利用小动物成像仪进行观察,待肿瘤荧光强度达到1.5E+06左右时将动物入组至对照组和治疗组(n=6)。
A. 肿瘤荧光强度±SEMB. 小鼠平均体重±SEM
结果显示:相同剂量下不同抗人CD47抗体对肿瘤生长的抑制效果不同。结果证明:B-NDG小鼠是评估人CD47抗体体内药效的有力工具。
***B-NDG B2m KO plus小鼠
(1)、B-NDG B2m KO plus小鼠能够有效延缓人PBMC移植导致的GvHD效应
B-NDG(n=10)和B-NDG B2m KO plus小鼠(n=5)尾静脉移植人PBMC(D1-3),根据对照表每周两次对GvHD 的临床体征进行评分。在 Prism 中分析数据。数值表示为平均值±SEM。**: P<0.01。结果显示:在人 PBMC移植的 GvHD 模型中,与 B-NDG 小鼠相比,B-NDG B2m KO plus小鼠显著延长了生存期,并且延迟 GvHD 的发生和降低其严重程度。
(2)、NCI-H226 CDX 肿瘤模型在 B-NDG B2m KO plus小鼠中进行的 CAR-T 体内疗效研究
CAR-T 疗法在B-NDG B2m KO plus小鼠中的抗肿瘤活性。将人 NCI-H226(1E7) 植入B-NDG B2m KO plus小鼠中。(A) 当肿瘤大小约为 150±50 mm3 时,对小鼠进行分组。此时,使用 CAR-T 细胞 (5E5) 按照图中所示的时间表进行处理。(B) 治疗期间的体重变化。
结果表明:CAR-T 细胞对 B-NDG B2m KO plus小鼠的肿瘤生长有不同的抑制作用。B-NDG 是人 CAR-T 细胞疗效研究的强有力模型。
***B-NDG hIL15小鼠
百奥赛图在重度免疫缺陷B-NDG小鼠基础上开发了B-NDG hIL15小鼠,基于此进行免疫重建及肿瘤建模,可以满足更多免疫研究需求,为依赖NK细胞或CD8+ T细胞发挥作用的抗体药物提供有力的评价模型。
(1)、B-NDG hIL15 小鼠人 PBMC 免疫系统植重建和 K562 CDX 模型生成
将人 PBMC 细胞 (5E6) 静脉植入纯合 B-NDG hIL15(雌性,6 周龄,n=5)和 B-NDG 小鼠(雌性,6 周龄,n=5)。K562 细胞 (1E6) 与 PBMC 同一天皮下植入 B-NDG hIL15 和 B-NDG 小鼠。(A) 肿瘤大小的平均值±SEM (B) 体重的平均值±SEM。K562 细胞在人 PBMC 免疫系统重建的小鼠模型上成功致瘤,与 B-NDG 小鼠相比,B-NDG hIL15 小鼠肿瘤生长明显延迟。
B-NDG hIL15 小鼠 PBMC 重建和 K562 CDX 模型生成后的 CD45 + 和 NK 细胞分析。将人 PBMC 细胞 (5E6) 静脉植入纯合 B-NDG hIL15(雌性,6 周龄,n=5)和 B-NDG 小鼠(雌性,6 周龄,n=5)。K562 细胞 (1E6) 与 PBMC 同一天皮下植入 B-NDG hIL15 和 B-NDG 小鼠。在不同时间取 B-NDG hIL15 和 B-NDG 小鼠血液进行流式细胞分析。与 B-NDG 相比,B-NDG hIL15 显示人 CD45 + 细胞百分比和人 NK 细胞的细胞数量更高。
(2)、B-NDG hIL15小鼠中的人PBMC免疫系统植入和PANC-1 CDX模型生成
将人PBMC细胞静脉植入纯合子B-NDG hIL15和B-NDG小鼠中。PANC-1细胞与PBMC同一天皮下植入B-NDG hIL15和B-NDG小鼠。(A)肿瘤大小的平均值±SEM;(B)体重的平均值±SEM;(C)在不同时间取B-NDG hIL15和B-NDG小鼠血液进行流式细胞分析。PANC-1细胞在人PBMC免疫系统重建的小鼠模型上成功致瘤,与B-NDG小鼠相比,B-NDG hIL15小鼠肿瘤生长明显延迟。与B-NDG相比,B-NDG hIL15显示人CD45 + 细胞百分比和人NK细胞数量更高。
(3)、PBMC免疫重建B-NDG hIL15小鼠胃癌模型评价CLDN18.2抗体药效
将人PBMC细胞(1E6)静脉植入纯合子B-NDG hIL15小鼠。将NUGC4-CLDN18.2(6E6)植入B-NDG IL15小鼠中。当肿瘤体积达到约70-100 mm3(n=5)时将小鼠分组,此时用IMAB362(in house)治疗,剂量和方案如图所示。(A)给药期间肿瘤体积变化,(B)给药期间体重变化。结果表明,在人PBMC免疫系统重建模型中,CLDN18.2抗体对B-NDG hIL15小鼠的肿瘤生长具有抑制作用。
(4)、PBMC免疫重建B-NDG hIL15小鼠黑色素瘤模型评价TIGIT抗体药效
将人PBMC细胞(1E6)静脉植入纯合子B-NDG hIL15小鼠。将A375(4E6)植入B-NDG hIL15小鼠体内。在肿瘤接种后第二天对小鼠进行分组(n=5),并按照图中所示的剂量和时间表给予Tiragolumab(in house)。(A)给药期间肿瘤体积变化,(B)给药期间体重变化。
结果表明,TIGIT抗体对人PBMC免疫系统重建模型B-NDG hIL15小鼠的肿瘤生长抑制有效。
如何选择免疫缺陷小鼠?
多种多样的免疫缺陷小鼠让我们在不同的研究领域或研究策略中可以灵活选择,这时需要从以下几个方面来综合考量:
遗传背景
小鼠的遗传背景,比如不同背景的小鼠H2单体型不同:裸鼠就有3种不同的背景:BALB/c Nude、Nu/Nu、CD-1 Nude。
其中BALB/c Nude为近交系,个体差异小,最常用于异种移植瘤模型的建立,成瘤所需肿瘤细胞接种量以及成瘤速度较后两者也都具有一定的优势;Nu/Nu和CD-1 Nude为封闭群,个体差异较大。
免疫系统组成成分
到底是需要哪种淋巴细胞缺陷的小鼠,还是多种免疫细胞共同缺失的?
T 淋巴细胞功能缺陷,例如:裸鼠
B 淋巴细胞功能缺陷,例如:CBA/N小鼠,带有Btk基因突变,是一种X连锁免疫缺陷,影响前B细胞的分化成熟,使B细胞功能缺陷,导致对胸腺非依赖性II型抗原无法作出抗体应答。血清中IgM和IgG含量降低,对B细胞分裂素缺乏反应,分泌IgM和IgG亚类的B细胞数量减少,其T细胞功能正常。
NK细胞功能缺陷,例如:Beige小鼠,Beige基因是13号常染色体隐性突变基因,表现为严重缺乏NK细胞,以及对同种、异种肿瘤细胞的细胞毒性T细胞和抗体应答减弱。较少单独在肿瘤学研究中应用。
联合免疫缺陷,例如:NOD-Scid小鼠、NSG小鼠等。
基于不同研究需求,南模生物自主研发了不同类型免疫细胞缺陷的基因工程小鼠(表1)以供广大科研工作者研究使用。
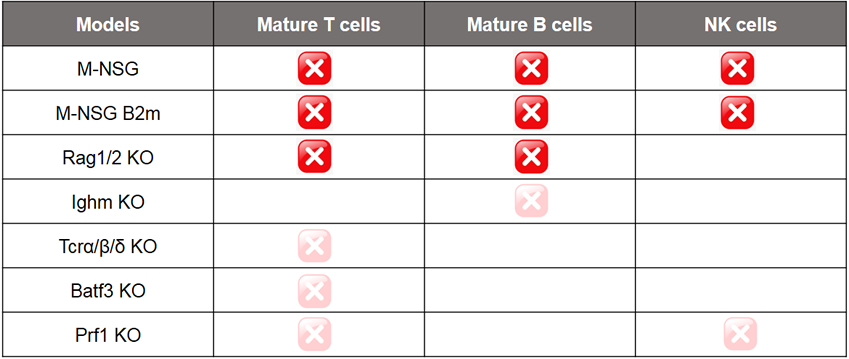
注:红色×表示Deleted,浅红色×表示 Reduced activity
突变基因
在研究过程中,考虑某个或某几个基因的突变对免疫反应的影响(如NK细胞,巨噬细胞和补体活性等),以及与遗传背景可能的相互作用。 例如,β2微球蛋白(B2m)和穿孔素(Prf1)突变会降低NK细胞活性;白介素2受体γ链(Il2rg)突变则使NK细胞完全失活;scid突变在NOD小鼠中抵抗糖尿病的发生。
免疫细胞的泄漏
有的免疫缺陷小鼠品系会随着年龄的增长,会产生一定程度的功能T、B细胞。
例如,不同遗传背景的scid突变小鼠,功能淋巴细胞的泄漏程度也不同:在 C57BL/6J 和 BALB/c 背景上泄漏率高;在C3H背景上较低;在NOD背景上极低。
寿命
有的免疫缺陷小鼠会自发淋巴瘤,导致小鼠寿命大幅缩短,因此不利于长期的跟踪实验。比如:Nod-Scid小鼠的寿命大约只有8-9个月。
辐照敏感度
对辐照特别敏感的免疫缺陷小鼠品系不适合在移植前进行辐照处理,比如:scid突变小鼠的辐照耐受量不超过400cGy (4 Gy)。
繁殖能力
例如:雌性裸鼠的繁殖能力很差,只有2.5月龄到4月龄的雌鼠才有生育能力。所以裸鼠的繁育是通过雄性纯合子与雌性杂合子来完成的。